You can find english version here.
Повышение эозинофильного катионного белка – одна из причин сосудистых заболеваний головного мозга и сопутствующих неврологических нарушений
Версия для людей без медицинского образования находится здесь.
Площадка для обсуждения находится здесь (только для мед. персонала и научных работников).
Ключевая идея: повышенный уровень эозинофильного катионного белка способствует возникновению спазмов сосудов головного мозга (под спазмом понимается временное сужение сосудов различной степени выраженности). Материал подготовлен человеком без медицинского образования и основан на личном опыте автора (см. раздел «Об авторе»).
Основной текст статьи написан в 2017 г., дополнения — в 2018-21г.
Содержание
- Аннотация
- Возможные симптомы
- Спазмы сосудов головного мозга
— факторы-триггеры
— факторы-условия - Нейротоксическое действие ЭКБ
- Связь повышенного уровня ЭКБ и спазмов сосудов
- Причины повышения ЭКБ и дополнительные комментарии
- Заключение
- Список литературы
- Приложение: дополнительные версии и наблюдения после написания статьи (период 2018-21)
- Предложение совместных исследований
Версия апр.2020: бактерии, близкие к риккетсиям
1. Аннотация
Разнообразные неврологические нарушения и сосудистые заболевания головного мозга (вплоть до дисциркуляторной энцефалопатии и инсульта) могут быть вызваны повышением в крови уровня эозинофильного катионного белка (англ. «ECP», для удобства чтения будет использоваться сокращение «ЭКБ»).
Эозинофильный катионный белок — небольшой белок, высвобождаемый из эозинофилов в результате определенных иммунных реакций. Повышение ЭКБ возможно при различных состояниях, связанных с аллергическими реакциями, бактериальными инфекциями, паразитарными инвазиями и т.п.
ЭКБ известен как нейротоксин, но автор статьи считает, что его влияние на мозг в большей степени связано не с прямым нейротоксическим действием, а с опосредованным — через воздействие на сосуды головного мозга. Автор предполагает, что повышенный уровень ЭКБ способствует возникновению спазма сосудов, что приводит к ишемии отдельных участков головного мозга и сопутствующим неврологическим нарушениям. Разнообразие возможных нарушений связано с тем, что в разные моменты времени от ишемии могут страдать различные участки головного мозга, что дает очаговую неврологическую симптоматику. Несмотря на временный характер нарушений, в долгосрочной перспективе заболевание, предположительно, может приводить к энцефалопатии в результате как гибели нейронов, так и утолщения сосудистой стенки.
Механизм влияния ЭКБ на сосуды может включать несколько факторов (подробное описание приведено в основном тексте статьи):
- изменение проницаемости клеточной мембраны и нарушение гомеостаза ключевых ионов (в т.ч. ионов кальция) в вегетативных нейронах и астроцитах, что приводит к неконтролируемому выделению медиатора (норадреналина), особенно при воздействии на шейный отдел позвоночника и шейные нервы;
- изменение проницаемости клеточной мембраны и нарушение гомеостаза ключевых ионов в гладкомышечных клетках сосудов, что нарушает механизм их сокращения и расслабления;
- повреждение сосудистой стенки, что приводит к дисфункции эндотелия сосудов и выбросу вазоактивных веществ при непосредственном воздействии на сосуды.
Нарушения возможны даже при умеренном повышении уровня ЭКБ (30-40 нг/мл при норме <24 нг/мл), без повышения эозинофилов и без гиперэозинофильного синдрома (это важно с точки зрения возможной распространенности подобных заболеваний). Вероятно, такое же влияние могут оказывать и родственные ЭКБ белки — основной кислый белок и (особенно) эозинофильный нейротоксин.
Возможные причины повышения ЭКБ: воспалительные процессы в кишечнике (в т.ч. вследствие избыточного бактериального роста в кишечнике, чувствительности к глютену, заболеваний печени и желчевыводящих путей), паразитарные инвазии, аллергические реакции, бактериальные инфекции (например, в носоглотке) и пр.
Таким образом, при наличии неврологических нарушений, причину которых не удается установить, предлагается проводить анализ ЭКБ. При повышенных значениях ЭКБ необходимо в первую очередь найти и устранить причину повышения (первичное заболевание). До устранения причины состояние может быть заметно улучшено приемом селективных блокаторов медленных кальциевых каналов (например, нимодипина) или α1-адреноблокаторов, а также минимизацией «факторов-триггеров», запускающих механизм спазма (подробнее описано в основном тексте статьи).
Практическая ценность статьи заключается в описании неочевидных причин неврологических нарушений, а также способа их своевременного выявления (через контроль уровня эозинофильного катионного белка).
Научная ценность заключается в описании механизма опосредованного воздействия эозинофильного катионного белка на головной мозг, который отличается от описанного в литературе непосредственного нейротоксического действия. Возможно, описанный механизм играет важную роль в возникновении ряда сосудистых заболеваний мозга.
Ограничения
Материал составлен человеком без медицинского образования, в связи с чем в изложении могут быть неточности. Автор будет рад любым комментариям и замечаниями, но призывает основное внимание уделить не деталям, а ключевой идее статьи.
В распоряжении автора нет достаточной базы для статистически надежных выводов. Выводы основаны на ряде научных статей (в части нейротоксического действия ЭКБ) и на собственных наблюдениях и экспериментах на фоне медицинских анализов. В западной практике можно встретить статьи, которые основаны на описании одного примечательного случая («case report»). Цель таких статей — не доказать что-либо, а обратить внимание медицинского и научного сообщества на значимые наблюдения. В этом заключается цель данной статьи.
Дополнительное ограничение накладывает тот факт, что автор был ограничен анализами, доступными в коммерческих лабораториях. Например, важную роль могут играть и другие белки, родственные ЭКБ — эозинофильный нейротоксин и основной кислый белок, но у автора не было возможности сдавать такие анализы. Аналогично, в доступных автору лабораториях чувствительность к глютену определяется по 6 анализам, тогда как в мировой практике используется значительно большее число анализов.
Ключевые слова
Эозинофильный катионный белок, транзиторная ишемическая атака, ишемический инсульт, спазмы сосудов головного мозга, очаговая неврологическая симптоматика, синдром позвоночного нерва, «вегетососудистая дистония», дисциркуляторная энцефалопатия, цереброваскулярная болезнь, gut-brain axis, воспаление кишечника, синдром избыточного бактериального роста, глютеновая энтеропатия, паразитарная инвазия.
2. Возможные симптомы
При изучении темы автор отталкивался от наблюдаемых симптомов, поэтому описание будет начато именно с них. Симптомы были очень разнообразны и, к тому же, менялись с течением болезни. В первый год заболевания (2011 год) было сложно четко описать симптоматику — в редкие дни было ощущение общей заторможенности (как при высокой температуре или похмелье) и ощущение повышенного внутричерепного давления. С течением времени симптомы становились более выраженными, и в то же время более разнообразными и четко определенными — то есть наблюдалась уже очаговая неврологическая симптоматика. Такие симптомы были временными (от нескольких минут до нескольких часов) и обратимыми. Симптомы могли наблюдаться независимо друг от друга. Со временем частота возникновения, разнообразие и тяжесть симптомов нарастали, и в худшие моменты (2014 год) можно было говорить о транзиторной ишемической атаке, граничащей с ишемическим инсультом.
Ниже приведен список возможных симптомов (группировка исключительно для удобства чтения, хотя возможна группировка и по месту локализации нарушения):
Умственные способности
- существенные затруднения при выполнении простой умственной работы, которая не представляет сложности в другие дни;
- существенное ухудшение памяти, затруднения при попытке вспомнить очевидные вещи (например, дату рождения);
- невозможность концентрации внимания;
- общая заторможенность.
Речь
- снижение четкости речи, неразборчивость речи, невозможность выговорить некоторые слова;
- несвязность, нелогичность речи, сложности с формулированием мыслей;
- подмена слов, невозможность вспомнить или подобрать нужное слово;
- сложность понимания речи других (вплоть до полной невозможности понять смысл простых предложений).
Общее состояние
- спутанность сознания (состояние как при очень высокой температуре, полуобморочное состояние);
- настроение, не адекватное ситуации (смешливость, эйфория, безэмоциональность и пр.).
Прочее
- боль в глазах (часто в одном), временное ухудшение зрения, двоение в глазах, расфокусировка зрения;
- ухудшение слуха (часто с одной стороны), шум в ушах;
- изменение мимики лица (маскообразность лица, опущенные уголки губ);
- неряшливость, неустойчивая походка;
- изменение почерка, пропуск букв в словах, очень частые опечатки при наборе текста.
Возможные сопутствующие симптомы
- ощущение напряжения в затылочной части головы;
- сухость и покраснение глаз;
- аллергические проявления неясной этиологии (дерматит, зуд и пр.);
- очень частая зевота, ощущение невозможности сделать полный вдох.
Как уже было сказано, симптомы наблюдались независимо друг от друга, то есть вполне возможным было состояние, когда автор легко выполнял умственную работу, но имел сложности с тем, чтобы внятно о ней рассказать. Свое состояние можно было «протестировать» выполнением простых операций, таких как умножение в уме, произнесение скороговорок, формулирование монолога на свободную тему и так далее. В разные моменты времени сложности возникали с разными операциями.
3. Спазмы сосудов головного мозга
Автор считает, что большая часть описанных неврологических нарушений была связана с ишемией отдельных участков головного мозга в результате спазма сосудов. К такой версии автора подтолкнуло исследование глазного дна (в заключении было сказано, что сосуды глазного дна несколько сужены), а также ощущение локализации нарушения — ощущения, что конкретные участки головного мозга страдают от ишемии (это чувствовалось, несмотря на отсутствие боли). При этом по результатам МРТ, ангиографии и других исследований органической патологии выявлено не было. Главным подтверждением версии спазмов сосудов стало очень выраженное улучшение состояния после приема селективных блокаторов медленных кальциевых каналов (БМКК) — нимодипина.
Говоря о спазмах сосудов, причину их возникновения представляется логичным разделять на две части (хотя автор не встречал такого деления в литературе):
- факторы-триггеры — факторы, запускающие механизм спазма (т.е. приводящие к немедленному спазму);
- факторы-условия — факторы, которые делают возможным запуск механизма спазма даже от незначительных факторов-триггеров. Так как от спазмов сосудов страдают не все люди, тогда как факторам-триггерам подвержены все — наличие именно этих факторов отличает больного человека от здорового.
Факторы-триггеры
Факторы-триггеры многочисленны и разнообразны.
Если рассматривать вопрос с точки зрения пациента, то факторами-триггерами могут выступать поворот головы, работа с сильно наклоненной головой (например, при чтении с бумаги или при работе с низко расположенным монитором), сон на слишком высокой/низкой подушке, вынужденная неудобная поза, тряская езда, неудобная одежда и так далее.
Значительная часть этих факторов так или иначе связана с шеей, а именно — с позвоночными артериями и/или шейными нервами (cervical nerves / нерв Франка). Шейные нервы оплетают позвоночные артерии и иннервирует сосуды мозга, составляющие бассейн позвоночных артерий [Малыхин, 2007], при этом в [Попелянский, 2003] было описано, что воздействие на нерв Франка (в том числе в результате травмы или заболеваний позвоночника) может приводить к рефлекторному спазму сосудов (синдром позвоночного нерва, или задний шейный симпатический синдром).
В советской и российской практике связь неврологических нарушений с состоянием позвоночника рассматривается такой ветвью неврологии, как вертеброневрология, основоположником которой был Я.Ю. Попелянский. Однако вертеброневрология часто подвергается критике, и, как считается, сейчас находится в кризисе — отчасти из-за того, что практические наблюдения не полностью соответствуют теоретической базе [Ахмадов, 2012]. Противоречия в вертеброневрологии были описаны еще учеником Я.Ю. Попелянского — профессором В.П. Веселовским — который в том числе отмечал «отсутствие параллелизма между степенью выраженности клинических проявлений и рентгенологических изменений при дистрофических поражениях позвоночника» [Ахмадов, 2012].
По личным наблюдениям автора, проблемы с шейным отделом позвоночника также не полностью объясняют наблюдаемые симптомы. Во-первых, по собственным наблюдениям, триггерами иногда могут выступать и события, не связанные с шейным отделом позвоночника, например, употребление большого количество сладкого (вероятно, играет роль сосудосуживающий эффект инсулина), курение (сосудосуживающий эффект никотина) или яркий свет. Во-вторых, в определенные моменты (конец 2014 года) спазмы возникали даже от чистки зубов или от малейшего поворота головы, тогда как в другие периоды — спазмы не возникали по несколько недель при наличии тех же факторов-триггеров. При этом существенных изменений в состоянии шейного отдела позвоночника не наблюдалось.
Таким образом, факторы-триггеры выполняют роль спускового крючка, но это лишь часть проблемы, а спазм сосудов происходит только при выполнении определенных условий.
Факторы-условия
Одним из первых направлений поисков факторов-условий было изучение ренин-ангиотензиновой системы. Предполагалось, что сбой именно в ее работе предрасполагает к спазмам. Если говорить конкретнее, предполагалось, что к спазмам располагает дисфункция эндотелия сосудов, при которой в случае воздействия на сосуды (в случае возникновения факторов-триггеров), сосудистая стенка может выделять вазоактивные вещества (эндотелин и ангиотензинпревращающий фермент), приводящие к спазму далее по кровеносному руслу.
В качестве одной из возможных причин дисфункции эндотелия автор рассматривал васкулит, связанный с аутоиммунными процессами. Но в это же время была замечена связь между усилением неврологических нарушений и различными аллергическими проявлениями неясной этиологии (дерматит, высыпания на коже головы, образование корок в носовой полости и пр.). Все это наталкивало на предположение об иммунно-аллергической природе заболевания, в результате чего автор среди прочих анализов сдал анализ на эозинофильный катионный белок, который оказался повышенным (колебался в районе 30-45 нг/мл при норме <24 нг/мл).
В данный момент автор статьи считает, что именно сам факт повышения уровня эозинофильного катионного белка является тем самым фактором-условием, которое делает возможным спазм сосудов даже в результате незначительного воздействия на сосуды и/или позвоночный нерв.
4. Нейротоксическое действие ЭКБ
Эозинофильный катионный белок — небольшой белок, высвобождаемый из эозинофилов в результате определенных иммунных реакций. Эозинофильный катионный белок является нейротоксином [Сорока, 1995; Fredens, 1982; Navarro et al., 2010]. Первоначальные сведения о нейротоксичности эозинофилов появились еще в 1930х годах, когда был описан «феномен Гордона» — неврологические нарушения у кроликов, которым была сделана инъекция взвеси лимфатических узлов человека, страдающего от болезни Ходжинга. Этот эффект связывался с наличием во взвеси эозинофилов. В дальнейшем было показано, что к «феномену Гордона» приводит и инъекция ЭКБ [Fredens, 1982].
К настоящему моменту описаны случаи быстрой деменции и раннего инсульта у людей с гиперэозинофильным синдромом [Briania et al., 2001; Kaplan, 2011; Nallegowda et al., 2003; Weaver, 1988]. Несмотря на это, механизм нейротоксического действия ЭКБ до сих пор изучен не полностью.
В исследовании [Navarro et al., 2010] приводятся следующие выводы по результатам ряда экспериментов:
- ЭКБ встраивается в мембрану клетки, изменяя ее проницаемость и нарушая внутриклеточный баланс ключевых ионов, влияющий на функционирование клетки. Это относится как к нейронам, так и к другим видам клеток [Navarro et al., 2007].
- ЭКБ запускает механизм апоптоза клетки (то есть механизм «нормальной», «программируемой» гибели).
- В экспериментах ЭКБ приводит к гибели как нейронов, так и астроцитов, при этом выживаемость клеток напрямую зависит от концентрации ЭКБ.
- Высокие концентрации ЭКБ приводят к резкому всплеску концентрации ионов кальция внутри нейрона/астроцита.
Утверждение об изменении внутриклеточного баланса ионов особенно важно в контексте обсуждения спазмов сосудов головного мозга.
5. Связь повышенного уровня ЭКБ и спазмов сосудов
Описанное в научных статьях непосредственное нейротоксическое действие ЭКБ не полностью объясняет наблюдаемые автором симптомы. По мнению автора статьи, главную роль в неврологических нарушениях играют именно спазмы сосудов головного мозга, которые, в свою очередь, также связаны с повышением уровня ЭКБ. Конечно, у автора нет возможности полноценно исследовать влияние ЭКБ на сосуды, но, предположительно, здесь может быть задействовано несколько механизмов:
- Изменение проницаемости клеточной мембраны и нарушение гомеостаза ключевых ионов, в т.ч. ионов кальция (в соответствии с [Navarro et al., 2007, 2010]), в вегетативных нейронах, что повышает их возбудимость и приводит к неконтролируемому выбросу медиатора — норадреналина, который имеет сильный сосудосуживающий эффект.Эта версия наилучшим образом сочетается с синдромом позвоночного нерва, то есть, предположительно, повышенный уровень ЭКБ делает шейные нервы более возбудимыми, что приводит к выбросу вазоконстрикторов в результате даже небольшого воздействия на шейный отдел позвоночника и шейные нервы.Эта версия хорошо описывает и личные наблюдения автора, в соответствии с которыми вероятность спазма зависит от текущего уровня ЭКБ. При нормальных уровнях ЭКБ спазм практически не возникает (независимо от наличия факторов-триггеров), при высоких — возникает при наличии малейших факторов-триггеров. При этом спазм может возникать в различных участках мозга — в зависимости от того, где произошел выброс норадреналина.
- Изменение проницаемости клеточной мембраны и нарушение гомеостаза ключевых ионов (в соответствии с [Navarro et al., 2007, 2010]) в гладкомышечных клетках сосудов, что нарушает механизм их сокращения и расслабления (в том числе под воздействием вазоактивных веществ). Сходный механизм был описан применительно к бронхам в [Madison et al., 2000]. В пользу этой версии говорит наличие факторов-триггеров, не связанных с шейным отделом позвоночника.
- Повреждение эозинофильным катионным белком сосудистой стенки, что приводит к дисфункции эндотелия сосудов. При дисфункции эндотелия при «механическом» воздействии на сосуды возможен выброс вазоконстрикторов и, как следствие, спазм далее по кровеносному руслу.Сам факт воздействия ЭКБ на сосуды отмечается в [Weaver, 1988; Сорока, 1995]. При этом в [Weaver, 1988] предполагается, что повреждение сосудистой стенки приводит к образованию тромбов и, как следствие, к эмболическим инфарктам мозга. Автор статьи в свою очередь предполагает другую причину ишемии — именно спазмы сосудов (без обязательного образования тромбов). Это принципиальное отличие, так как это подразумевает использование других терапевтических средств (блокаторы медленных кальциевых каналов и α1-адреноблокаторы).В пользу этой версии говорит факт постепенного нарастания симптомов (возможно постепенное повреждение эндотелия). Однако против этой версии говорит то, что спазм возникает в различных участках мозга — тогда как если бы это было основной причиной, то в случае поворота головы вазоконстрикторы всё время выделялись бы в одном месте позвоночной артерии — и оказывали бы влияние на одни и те же участки мозга. Кроме того, было замечено, что наибольший спазмолитический эффект оказывали блокаторы медленных кальциевых каналов и α1-адреноблокаторы, тогда как прием ингибиторов ангиотензинпревращающего фермента и антагонистов рецепторов ангиотензина-II не давали заметного результата (то есть проблема с меньшей вероятностью связана с выбросом ангиотензинпревращающего фермента).
- Нарушение гомеостаза ключевых ионов (в соответствии с [Navarro et al., 2007, 2010]) в астроцитах, которые также способны выделять вазоактивные вещества. В пользу этого механизма говорит общее ухудшение состояния при повышении уровня ЭКБ, даже при отсутствии явных факторов-триггеров и при отсутствии ощущения локализации нарушения.
Вероятно, такое же влияние может оказывать и родственный ЭКБ белок — эозинофильный нейротоксин, который обладает свойствами, в значительной степени сходными со свойствами ЭКБ [Gleich G. et al., 1986; Navarro S. et al., 2010].
Независимо от того, какой именно механизм здесь играет главную роль, все они предрасполагают к возникновению спазмов сосудов головного мозга. Кроме того, несмотря на транзиторный характер спазмов, представляется вполне очевидным, что в долгосрочной перспективе они могут приводить к энцефалопатии в результате как гибели нейронов, так и утолщения сосудистой стенки.
6. Причины повышения ЭКБ и дополнительные комментарии
*Несмотря на общий предполагаемый механизм связи ЭКБ и неврологической симптоматики, первопричины повышения ЭКБ могут быть различными. Раздел будет содержать меньше ссылок на литературу и больше собственных наблюдений (учитывая индивидуальность возможных причин). Информация может дополняться и корректироваться.*
Причины повышения ЭКБ могут быть достаточно индивидуальны, поэтому выявление одной-единственной причины, актуальной для всех пациентов, не является целью этого раздела. К повышению ЭКБ может приводить множество факторов, и, к сожалению, они также не всегда очевидны.
В литературе/интернете чаще всего перечисляются следующие основные причины повышения ЭКБ:
- паразитарные инвазии;
- аллергические реакции;
- бактериальные инфекции;
- бронхиальная астма;
- аутоиммунные процессы.
Реже к списку добавляется язва или воспаление кишечника, а также другие заболевания желудочно-кишечного тракта.
Рассмотрим подробнее основные причины (на опыте автора). При этом можно будет заметить, что некоторые причины повышения ЭКБ в литературе уже ассоциируются с различными неврологическими нарушениями (само повышение ЭКБ при этом не упоминается). То есть повышение ЭКБ объединяет различные заболевания, которые могут давать неврологическую симптоматику.
Паразитарные инвазии
Паразитарная инвазия была первой версией автора (в последствие не подтвердилась). ЭКБ токсичен для гельминтов [Сорока, 1995] и повышается при большинстве паразитарных инвазий. Что интересно, как ведущие, так и рядовые сотрудники центра паразитологии Марцинковского (г. Москва) не были удивлены возможной связью неврологических нарушений с паразитами. Для паразитологов неврологические нарушения при инвазиях являются достаточно известными и очевидными. Важно, что к такому эффекту приводят не только редкие паразиты, локализующиеся непосредственно в головном мозге, а все наиболее распространенные виды. Неврологические нарушения при этом связывают именно с их токсическим влиянием на организм.
Таким образом, первое, на что можно сдать анализ в случае повышения ЭКБ (особенно у детей) — это анализ на наиболее распространенных паразитов.
Аллергические реакции
Следующей версией автора была скрытая аллергическая реакция. Были сданы анализы на все основные аллергены (респираторные и пищевые панели), но результат не давал оснований говорить об аллергии.
Однако впоследствии оказалось, что пищевые панели не позволяют достаточно точно выявить одну из распространенных пищевых аллергий — чувствительность к глютену. Чувствительность к глютену определяется целым рядом специфических анализов, в российских лабораториях используется около 6 анализов, на западе — до 24 (CYREX массив 3). Возможно, именно поэтому на западе чувствительность к глютену выявляется значительно чаще. Кроме того, необходимо отметить, что в соответствии с современными представлениями о чувствительности к глютену, это заболевание уже не считается редким, а распространенность ее скрытых форм может достигать 1:100 [Парфенов, 2013], а по некоторым данным — 1:3 [Перлмуттер, 2014]. При этом скрытые формы часто «маскируются» под другие заболевания.
Как оказалось, связь чувствительности к глютену с неврологическими нарушениями на западе уже также известна и была описана, например, в [Перлмуттер, 2014]. Однако в [Перлмуттер, 2014] предполагается другой механизм влияния на мозг — без участия ЭКБ и спазмов сосудов.
Таким образом, при повышении ЭКБ стоит также сдать анализы на чувствительность к глютену и, при необходимости, на другие аллергены (пищевая и респираторная панели).
Вопрос, есть ли у автора статьи чувствительность к глютену, пока остается открытым. Из шести анализов — пять в пределах референсных значений и один постоянно повышен. Однако биопсия не подтвердила наличие глютеновой энтеропатии, а результаты генетических исследований также говорят о ее маловероятности. Безглютеновая диета не повлияла на динамику ЭКБ, хотя здесь есть нюансы, которые описаны ниже (в разделе «Дополнительные комментарии»).
Воспаление кишечника (в результате дисбактериоза)
В то же время, по результатам биопсии было выявлено воспаление кишечника (хронический дуоденит и хронический эрозивный колит), предположительно, имеющее бактериальную природу (по результатам анализов было выявлено развитие условно-патогенной и патогенной микрофлоры). Воспаление кишечника также может приводить к повышению ЭКБ, и это было основной версией автора на момент написания статьи (2017 год).
Здесь необходимо отметить следующие наблюдения:
— в середине 2014 года автор наблюдал самый значительный период ремиссии (полное отсутствие неврологических нарушений). В тот момент у автора не было версии ни про спазмы, ни про ЭКБ, однако было подмечено, что это произошло после курса антибиотиков (в связи с другим заболеванием);
— в конце 2014 года у автора был период самых частых, тяжелых и продолжительных неврологических нарушений — при этом, предположительно, после курса антибиотиков в середине года не была полностью восставлена микрофлора кишечника, тогда как недостаток бифидо- и лактобактерий приводит к развитию патогенной микрофлоры;
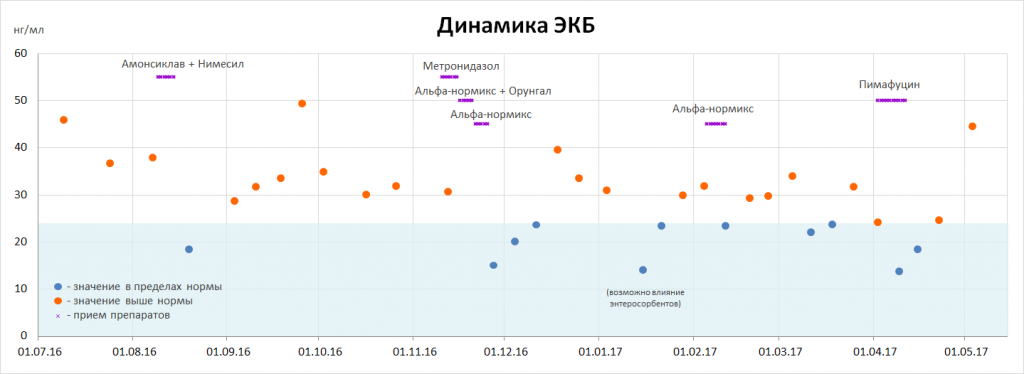
— в авг.16 после лечения антибиотиками другого заболевания ЭКБ снизился, но восстановился в течение следующих недель (см. диаграмму ниже);
— в ноя.16 после выявления воспаления кишечника лечение антибиотиками также привело к снижению ЭКБ, однако его уровень также восстановился в течение следующих недель;
— в апр.17 прием противогрибкового средства Пимафуцин (против грибов рода Candida, развитие которых было выявлено в анализе на дисбактериоз), действующего исключительно в кишечнике, также привело к резкому снижению ЭКБ (однако есть вероятность, что снижение было связано не столько с устранением грибов рода Candida, сколько с выводом ЭКБ из кишечника в результате побочных эффектов Пимафуцина; так или иначе, связь ЭКБ с кишечником представляется достаточно наглядной).
Таким образом, при повышении ЭКБ стоит также сдать анализы на дисбактериоз (стоит заметить, что для описания дисбактериоза в англоязычной практике используется термин «(Small) Intestinal Bacterial Overgrowth», подчеркивающий развитие избыточной микрофлоры в (тонком) кишечнике). Если выявлено развитие условно-патогенной и патогенной микрофлоры, больному стоит обратиться к гастроэнтерологу. Пока баланс микрофлоры не восстановлен, уменьшить влияние ЭКБ (и эндотоксинов, ассоциированных с развитием патогенной микрофлоры) возможно приемом энтеросорбентов (например, Энтеросгеля). Кроме того, необходимо помнить, что после использования антибиотиков необходимо полноценно восстанавливать микрофлору кишечника и следить за ее состоянием даже при отсутствии жалоб с точки зрения ЖКТ.
Впоследствии оказалось, что связь микрофлоры кишечника с мозгом также уже описывалась, см. литературу по ключевым словам gut-brain axis (на русский язык переведено [Перлмуттер, 2017]). Однако в этой литературе описывается другой механизм связи (без участия ЭКБ и спазмов сосудов).
Воспаление кишечника (в результате заболеваний органов ЖКТ)
В то же время, развитие патогенной микрофлоры может быть лишь следствием воспаления кишечника, а не причиной. Другая возможная причина воспаления кишечника — заболевания органов ЖКТ, в т.ч. печени и желчевыводящих путей. Что примечательно, есть отдельный термин, связывающий нарушения работы мозга с заболеваниями печени — «печеночная энцефалопатия». Неврологические нарушения при этом также связывают с повышением в крови определенных токсических веществ. Поэтому пациенту также стоит сдать соответствующие анализы — АлАТ, АсАТ, Гамма-ГТ, Билирубин. У автора перечисленные анализы также находятся в пределах нормы (единственный анализ вне референсных значений — желчные кислоты, но установить «диагностическую ценность» этого анализа пока не удалось).
Несмотря на то, что выявить причину воспаления кишечника автору найти не удалось, зависимость уровня ЭКБ от состояния кишечника достаточно заметна (именно у автора).
Другие причины
Другие возможные причины повышения ЭКБ:
- прочие заболевания желудочно-кишечного тракта (в т.ч. язва кишечника);
- другие бактериальные инфекции (например, в носоглотке);
- другие аллергические реакции;
- бронхиальная астма;
- аутоиммунные заболевания.
Так как причины достаточно индивидуальны, вероятно, для выдвижения дополнительных версий стоит отталкиваться от анамнеза пациента.
Дополнительные комментарии
*Информация может дополняться и корректироваться*
- На протяжении всего периода наблюдений эозинофилы были в норме. ЭКБ колебался в районе 30-50 нг/мл (при норме <24 нг/мл). То есть описанный случай не относится к достаточно редким гиперэозинофильным синдромам. Это важно с точки зрения возможной распространенности подобных заболеваний.
- На протяжении практически всего периода наблюдений был повышен уровень мочевой кислоты (причем после лечения воспаления кишечника он также снизился). Что интересно, имеются сведения о защитном влиянии мочевой кислоты при ишемии мозга [Mattson M. et al., 2000].
- Из всех анализов крови (очень большой список) — стабильно повышенные значения были только по ЭКБ, мочевой кислоте и антителам к деамидированным пептидам глиадина IgA (анализ для выявления чувствительности к глютену; в 2019 году появились оноснования полагать, что повышенные уровни этого анализа были ошибкой лаборатории). Биохимия печени в норме (кроме желчных кислот), щитовидная железа в норме.
- Динамика антител к деамидированным пептидам глиадина IgA не полностью объяснялась диетой. При употреблении глютен-содержащих продуктов результат мог оказаться достаточно низким, при соблюдении диеты — достаточно высоким. Не исключено, что чувствительность к глютену может быть также связана с состоянием микрофлоры кишечника [Barcik W. et al., 2016; Caminero A. et al., 2015]. По наблюдениям автора от состояния микрофлоры кишечника зависели результаты и других анализов, которые часто были вне референсных значений. В нескольких случаях, когда анализ на дисбактериоз не выявлял никаких нарушений, в норму приходили и ЭКБ, и мочевая кислота, и антитела к деамидированным пептидам глиадина, и желчные кислоты.
- Результаты анализа на дисбактериоз были нестабильны во времени и сильно менялись даже за одну неделю. Однако было замечено, что ухудшение состояния и повышение ЭКБ было возможно и без избыточного роста грамотрицательных бактерий. Это говорит о том, что влияние микрофлоры кишечника на мозг связано не только с липополисахаридами, которые являются результатом распада именно грамотрицательных бактерий (что было версией нескольких неврологов, к которым обращался автор).
- В дополнение к наблюдению «вероятность спазма зависит от текущего уровня ЭКБ»: чтобы оценка состояния была более объективной и не менялась постфактум в зависимости от результатов анализов, начиная с мая 2017 года используется следующая схема — в день сдачи анализа и до получения результата дается оценка уровня ЭКБ, сделанная на основе своего состояния за день/неделю. Таким образом, оценка становится более объективной — оцифрованной, фиксированной и не зависящей от результатов анализа. Результат приведен на графике ниже:
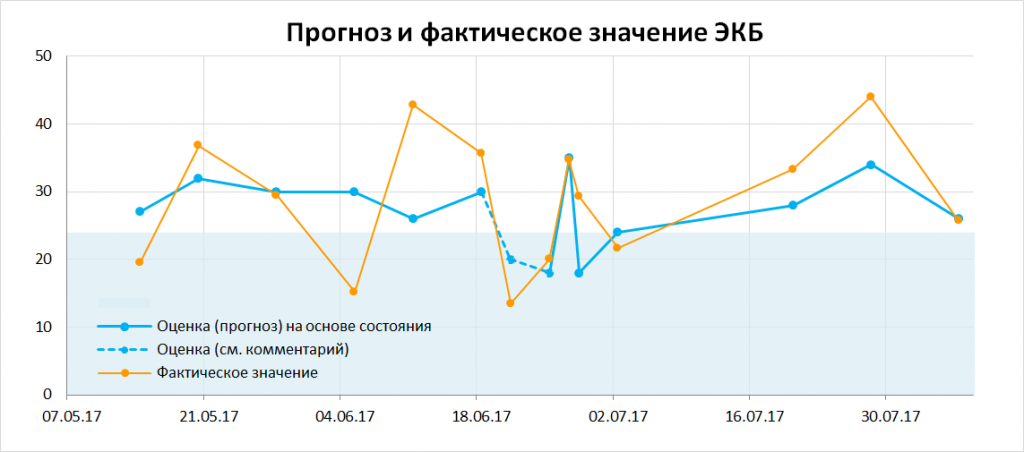 В момент сдачи анализа 21 июня точной оценки уровня ЭКБ не делалось, значение проставлено постфактум (отмечено штриховой линией), однако состояние в этот день было особенно хорошим, из-за чего и было принято решение сдать анализ внепланово (в рабочий день). Как видно из графика, несмотря на существенное расхождение в отдельные дни (5 и 11 июня), корреляция между оценкой состояния и уровнем ЭКБ достаточно высока.
В момент сдачи анализа 21 июня точной оценки уровня ЭКБ не делалось, значение проставлено постфактум (отмечено штриховой линией), однако состояние в этот день было особенно хорошим, из-за чего и было принято решение сдать анализ внепланово (в рабочий день). Как видно из графика, несмотря на существенное расхождение в отдельные дни (5 и 11 июня), корреляция между оценкой состояния и уровнем ЭКБ достаточно высока.
[Upd. 2021: дальнейшая динамика (2017-21) не однозначная, наблюдалось постепенное повышение уровня ЭКБ без нарастания симптомов]
- Несмотря на то, что устойчивого снижения ЭКБ автору добиться не удается, состояние радикально улучшено благодаря приему нимодипина (Нимотоп производства BAYER), контролю факторов-триггеров и коррекции диеты. Вполне вероятно, что средний уровень ЭКБ до конца 2014 года был существенно выше (когда были наиболее тяжелые симптомы), однако, к сожалению, подтвердить это уже не удастся.
7. Заключение
Таким образом, с одной стороны, повышение ЭКБ может играть ключевую роль в развитии ряда сосудистых заболеваний головного мозга (и сопутствующих неврологических нарушений), с другой стороны — повышение ЭКБ объединяет целый ряд заболеваний, которые сопровождаются неврологической симптоматикой. Поэтому независимо от причины повышения ЭКБ, которая может быть очень индивидуальной, анализ на ЭКБ представляется универсальным диагностическим средством, которое может широко использоваться в неврологии.
В [Угрюмов М.В., 2014] отмечалось, что в подавляющем большинстве случаев причина хронических нейродегенеративных заболеваний остается неизвестной. Автор статьи надеется, что влияние ЭКБ поможет объяснить целый пласт цереброваскулярных заболеваний, что позволит предотвратить их развитие у значительного количества людей.
Предлагаемая схема работы
При наличии неопределенных неврологических жалоб («вегетососудистая дистония» и пр.), снижении умственных способностей, различных неврологических нарушениях, причину которых не удается установить, предлагается направлять на анализ эозинофильного катионного белка. В случае повышенных значений, в первую очередь необходимо выявить и устранить первичное заболевание. Пока сохраняются симптомы, состояние может быть заметно улучшено:
- приемом селективных БМКК (ниподипина); возможно, кому-то также подойдут α1-адреноблокаторы (однако нужно иметь в виду, что α1-адреноблокаторы, являющиеся производными алкалоидов спорыньи, включая Сермион и Вазобрал, в Европе уже не рекомендуются к применению из-за возможных отложенных побочных эффектов [EMA, 2013]);
- минимизацией факторов-триггеров (например, сон только на спине на невысокой ортопедической подушке, избегание резких поворотов/наклонов головы, отказ от курения и т.п.);
- при необходимости (в зависимости от предполагаемой причины) — приемом противовоспалительных средств, антигистаминных средств для снижения степени сенсибилизации, энтеросорбентов для снижения уровня ЭКБ и эндотоксинов в кишечнике. Также эффект может оказать гинкго билоба (благодаря снижению вязкости крови).
Кроме того, учитывая хронический и часто скрытый характер нейродегенеративных заболеваний, автор считает, что анализ на ЭКБ стоит того, чтобы быть включенным в программы диспансеризации для контроля даже при отсутствии жалоб.
8. Список литературы
- Alfadda A., Storr M., Shaffer E., Eosinophilic colitis: epidemiology, clinical features, and current management. Therapeutic Advances in Gastroenterology, (2010) 4(5) 301-309
- Barcik W., Untersmayr E., Pali-Scholl I., O’Mahony L., Frei R., Influence of microbiome and diet on immune responses in food allergy models, DDMOD-428, 2016
- Briania C., Baracchinia C., Zanetteb G., Zanussob G., Carolloc C. and Monacob S., Rapidly progressive dementia in hypereosinophilic syndrome. European Journal of Neurology 2001, 8: 279-280
- Bystrom J., Amin K., Bishop-Bailey D., Analysing the eosinophil cationic protein — a clue to the function of the eosinophil granulocyte. Bystrom et al. Respiratory Research 2011, 12:10
- Caminero A., Nistal E., Differences in gluten metabolism among healthy volunteers, coeliac disease patients and first-degree relatives. British Journal of Nutrition (2015), 114, 1157–1167
- European Medicines Agency (EMA), New restrictions on use of medicines containing ergot derivatives, press release 28.06.2013
- Fredens K., Dahl R., Venge P., The Gordon phenomenon induced by the eosinophil cationic protein and eosinophil protein X. J Allergy Clin Immunol 1982, 70(5):361-366.
- Gleich G., Loegering D., Bell M., Checkel J., Ackerman S., McKean D., Biochemical and functional similarities between human EDN and ECP. Proc. Natl. Acad. Sci. USA Vol. 83, pp. 3146-3150, 1986
- Kaplan P., Central Nervous System Problems With Eosinophilia. Arch Neurol / Vol 68 (No 12), dec.2011
- Kazuko Shichijo, Kazuya Makiyama et al., Antibody to eosinophil cationic protein suppresses dextran sulfate sodium-induced colitis in rats. World Journal of Gastroenterology 2005;11(29):4505-4510
- Madison M., Schramm C., Cationic Proteins and Bronchial Hyperresponsiveness. American Journal of Respiratory Cell and Molecular Biology Vol. 22 2000
- Mattson M., Culmsee C., Zai Fang Yu, Apoptotic and antiapoptotic mechanisms in stroke. Cell Tissue Res (2000) 301:173–187
- Nallegowda M., Singh U., Handa G., Arora B., Idiopathic Hypereosinophilic Syndrome with Stroke in Young: A Case Report. IJPMR 14, April 2003; 24-26
- Navarro S., Aleu J., Jimenez M., Boix E., Cuchillo C. M., Nogues M. V., The cytotoxicity of eosinophil cationic protein/ribonuclease 3 on eukaryotic cell lines takes place through its aggregation on the cell membrane. Cell. Mol. Life Sci. 65 (2008) 324 – 337
- Navarro S., Boix E., Cuchillo C., Nogués V., Eosinophil-induced neurotoxicity: The role of eosinophil cationic protein/RNase 3. Journal of Neuroimmunology 227 (2010) 60–70
- Smaili S., Hirata H. et al., Calcium and cell death signaling in neurodegeneration and aging. An Acad Bras Cienc (2009) 81 (3)
- Stetka B., Perlmutter D., Dementia: Is Gluten the Culprit? Medscape. Jan 21, 2014.
- Vivian A., Salazar M., Exploring The Mechanism of Action of Human Antimicrobial Ribonucleases. Barcelona, 2015
- Weaver D.F., Heffernan L.P., Purdy R.A., Ing V.W., Eosinophil-induced neurotoxicity: Axonal neuropathy, cerebral infarction and dementia. Neurology 1988;38:144-146
- Wojda U., Salinska E. and Kuznicki J., Calcium Ions in Neuronal Degeneration. IUBMB Life, 60(9): 575–590, September 2008
- Yamasaki K., Makiyama K., Eosinophil Cationic Protein (ECP) in Ulcerative Colitis. Acta Med. Nagasaki 39: 67-71
- Ахмадов Т.З., Существует ли кризис в вертеброневрологии (организационные и методологические аспекты изучения проблемы остеохондроза позвоночника), Чеченский государственный университет, 2012
- Малыхин А.В., Вегетативные пароксизмальные состояния и терморегуляция организма
- Парфенов А.И., Глютенчувствительная целиакия – мультидисциплинарная патология человека. Верхневолжский медицинский журнал, 2013 — т.11, вып. 2.
- Перлмуттер Д., Еда и мозг (перевод с английского). Изд. «Манн, Иванов и Фербер», 2014
- Перлмуттер Д., Лоберг К., Кишечник и мозг (перевод с английского). Изд. «Манн, Иванов и Фербер», 2017
- Попелянский Я.Ю., Ортопедическая неврология (вертеброневрология), «МЕДпресс-информ», издание 2011
- Сорока Н.Ф., Савченко М.А., Современные представления о роли эозинофолов в организме и гиперэозинофильных синдромах. Журнал «Медицинские новости», №3, 1995
- Угрюмов М.В., Болезни мозга: как спасти нейроны (интервью), Harvard Business Review, 2014
Приложение: дополнительные версии и наблюдения после написания статьи (период 2018-21)
Версии (относительно первопричины нарушений конкретно у автора статьи)
- хронический клещевой боррелиоз (болезнь Лайма) — отвергнута [2018]; [2021: анализы противоречивы]
- пониженная кислотность желудка — отвергнута;
- болезнь Крона — отвергнута;
- болезнь Уиппла — отвергнута (не подтверждена по биопсии);
- нарушение обмена пуринов и пиримидинов — отвергнута;
- гиперчувствительность к определенным пищевым добавкам (в частности, E211) — наблюдения неоднозначны;
- «повышенная потребность» в никотиновой кислоте (витамин B3) — наблюдения неоднозначны;
- нарушение аминокислотного обмена — под вопросом;
- «повышенная проницаемость кишечника» — под вопросом;
- сифилис — отвергнута.
- бактерии, близкие к риккетсиям — под вопросом.
Наблюдения
- C-реактивный белок на протяжении всего периода наблюдений был в норме.
- май.18, май.20, янв.22: после употребления пищи с усилителем вкуса E621 (глутамат натрия) появляется ощущение распирания головы, раздраженное/озлобленное состояние.
- сен.18: после употребления пищи с консервантом Е211 (бензоат натрия) иногда возникает заторможенное состояние. После эпизода ОЧЕНЬ сильного затормаживания (был на обеде со знакомой, начало разговора было нормальным, к концу обеда реакция на реплики в разговоре стала с задержкой в 1-2 сек.). Для подтверждения связи с E211 на следующий день был сдан анализ мочи на органические кислоты. В результате была повышена только Гиппуровая кислота (519.69 ммоль/моль креат. при референсных значениях 60.00 — 300.00), которая является производным бензойной кислоты.
- мар.19: после применения препарата Бисептол уровень ЭКБ упал к нулевым значениям (восстановился через неделю). Возможно побочное действия препарата на кроветворную систему (при условии, что здесь нет ошибки лаборатории).
- апр.19: был эпизод «кровавого пота» (гематидроз). Эпизод был ночью, при этом стресса, страха и т.п. (которые, как пишут, могут быть триггерами такого явления) в тот день абсолютно точно не было.
- июн.19: замечено, что при напряжении мышц шеи и ощущении спазмированности шейных артерий, заметное улучшение происходит практически сразу (10 мин.) после употребления очень острой еды (перец чили). Возможно за счет раздражающего влияния на блуждающий нерв.
- фев.21, июл.21: обнаружен один из маркеров болезни Лайма (антитела к антигенам Osp, p31), при отсутствии остальных маркеров (итоговый вывод лаборатории по болезни Лайма — отрицательно).
- июн.21: на протяжении длительного времени (возможно, несколько лет) есть обильные высыпания на спине и груди (акне). Раньше не проводил связи высыпаний на теле с ЭКБ, но в 2014 году, в период максимальной выраженности симптомов, как минимум обращал внимание на высыпания на голове (возможно, связь с риккетсиями? см. описание ниже).
- июл.21: повышен иммунорегуляторный индекс (CD3+CD4+/CD3+CD8+), значения в районе 3-3.5 (анализы от июл.16, май.19, июл.21).
Версия апр.2020: бактерии, близкие к риккетсиям
Описание версии в личной переписке (к сожалению, сейчас нет времени/сил «облагородить» текст):
Короче, новая версия насчет моей головы. Самая реалистичная, самая основательная, в которую укладываются почти все разнообразные наблюдения за многие годы. Есть бактерии — риккетсии, вот я теперь думаю, что всё из-за них или им подобных. Их много видов, один из них вызывает сыпной тиф (тифов тоже много, вызываемых разными бактериями). И один из симптомов тифа — неврологические нарушения. Но это звучит не конкретно и не убедительно, ок.
Основной момент в том, что эта бактерия укладывается одновременно в две линии моих теоретических размышлений.
Первая линия — по пути «дисфункции эндотелия сосудов», из-за которой эндотелий высвобождает вазоконстрикторы от любого чиха (типа поворота головы), что приводит к спазму дальше по кровеносному руслу.
Риккетсия в эту тему укладывается на 1460%. Для начала в вики пишут: «Риккетсии обладают тропизмом к клеткам эндотелия сосудов.», на странице про тиф: «часто внедряются в эндотелиальные клетки сосудов». И в других местах интернета: «В организме человека их выявляют в клетках, которые выстилают поверхность кровеносных сосудов, благодаря чему могут вызывать проблемы их воспаления, закупорки или кровоизлияния.»Вторая линия (моих размышлений насчет головы) — по пути «эндотоксинов», которые выделяются при разложении грам-отрицательных бактерий. Эта линия была связана с тем, что в некоторые периоды у меня было постоянно мутное состояние, какое-то полуобморочное, как при сильном похмелье, и это без всяких поворотов головы. Поэтому я проверял теорию связи с ЖКТ и т.п. — т.к. «эндотоксиновая агрессия» возможна при всяких там «синдромах избыточного бактериального роста» в ЖКТ.
И, о чудо!, эта бактерия именно грам-отрицательная. И часть симптомов, которые описываются при сыпном тифе, как раз больше похожи на это общее мутное состояние, а не на спазм в конкретном участке мозга.При этом (пока не исследовано, но как зацепки):
- Про нее пишут, что это «внутриклеточный паразит», имея в виду, что она встраивается в клетки сосудов. Это типа как промежуточное звено между вирусами и бактериями. И вот внимание цепляется за слово «паразит» — т.к. про пресловутый эозинофильный катионный белок в первую очередь пишут, что он повышается при паразитах. Уж хз, есть ли здесь что-то общее с точки зрения иммунитета и т.п., но совпадение мощное.
- Года 3 назад заметил, что у меня болит голова после глутамата натрия. Ну болит и болит, перестал его есть и ладно. И что же мы теперь видим у риккетсий?… «Источником энергии у внеклеточных риккетсий служит глутамат.». Уж тоже не знаю, насколько это связано, но слишком уж много совпадений.
- Как знать, как знать, может наличие такой фигни в клетках сосудов и привело к кровавому поту в том году?…
Теперь, откуда она у меня может быть. Она передается трансмиссивным путем, то есть всякими кровососами. И вот тут на сцену выходят клещи. Я не знаю сколько, но в детстве у меня были клещи, может 3-10, точно не знаю. И клещей ни разу не отдавали на анализ. И антибиотиков я не пил. Ладно, энцефалита может в *** *** нет, но другие заболевания — хзхз. Вероятность, что клещи хоть чем-то болели, явно далека от нуля (тем более, что когда и я, и брат в 2018 хватали клещей, у обоих клещей какие-то болезни были).
И еще ладно эти 3-10 клещей. У моей кошки было, наверно, >50 клещей. Ну были и были, казалось бы. Но я точно помню один момент в детстве, когда у нее (у кошки) расплодились очень злые блохи, и помню момент, когда почувствовал сам этих блох, как они меня кусанули. Это тоже плюс к вероятностям.
Допускаю, что у меня не конкретно риккетсии, но что-то очень близкое по сути. Или риккетсии, но какого-то отдельного вида (не тот же, что вызывает сыпной тиф). И есть более-менее объяснение, почему они относительно не изучены — это очень небольшие бактерии. Плюс ту же болезнь Лайма (клещевой боррелиоз) тоже выявили совсем недавно, в 1975 году.
Вот так вот.
Один анализ на риккетсий уже сдавал — сказали нет. Но во-первых, возможно этот анализ заточен под конкретный вид риккетсий, во-вторых, возможно он срабатывает при более остром течении. Ну и в-третьих, да, возможно это не сами риккетсии, но что-то очень похожее.Теперь думаю, как и куда сдать на исследование под микроскопом кусочек своих позвоночных артерий (из шеи)…
… (шутка, в которой есть доля шутки…)Единственное, что пока не укладывается в картину — пишут, что риккетсии очень чувствительны к антибиотикам, в т.ч. доксициклину. А я в 2018 (после того клеща) использовал просто лошадиные дозы антибиотиков (и доксициклина). Но возможно это зависит от стадии (в целом так же, как с боррелиозом).
А насчет «линий размышлений» (дисфункция эндотелия и эндотоксины) — это помимо ЭКБ. Можно сказать, размышления с другой стороны.Я понимаю, что это может оказаться фигней, что могут быть незамеченные не стыковки и т.п. У меня уже столько теорий было, что к новым я уже не отношусь как к единственно верным, в которых я на 100% уверен. Но пока явных противоречий не вижу. И даже если какой-нибудь врач скажет, что всё это херня — опять-таки, эта не такая изученная область (если уж не так давно нашли боррелиоз), поэтому и врач может не знать..
Предложение совместных исследований
Если вы являетесь студентом мед. вуза, научным работником и др., и вас заинтересовала тема, описанная в статье, возможно проведение совместных исследований.
Например, для подтверждения/опровержения версии наличия бактерии, близкой к риккетсиям, можно использовать лабораторных мышей — «заразить» моей кровью и через несколько месяцев исследовать их сосуды. Результат, конечно, не гарантирован.
Открыт и к другим вариантам исследования.
Если вы заинтересованы, напишите мне на mbrain16@outlook.com.
Об авторе
В 24 года (2010-11г.) я начал замечать у себя различные временные неврологические нарушения (описаны в статье). С тех пор я посетил огромное количество врачей различных специальностей, однако причина нарушений оставалась неизвестной. Множество исследований не давало оснований говорить об органической патологии, а все анализы, которые мне предлагалось сдать, были также в пределах нормы.
Проблема сохранялась, снижая качество жизни и угрожая карьере. Поэтому я продолжал искать причину самостоятельно, основываясь на личных наблюдениях и экспериментах с лекарствами (на фоне большого количества медицинских анализов), а также на ряде научных статей. Эта статья — результат моих поисков.
Я понимаю, что предположение о роли эозинофильного катионного белка может оказаться ошибочным, но считаю, что мои выводы стоят того, чтобы их кто-то верифицировал. В любом случае, я верю, что мой материал может быть полезен неврологам, нейрофизиологам и прочим специалистам.
Любые вопросы и комментарии можно направлять на адрес mbrain16@outlook.com.